化学试卷
注意事项:本试卷共6页,总分60分,考试时间60分钟。
可能用到的相对原子质量:H-1C-12O-16Na-23Cl-35.5
一、选择题(本大题共10小题,每小题2分,共20分。在每小题给出的四个选项中,只有一项最符合题意)
1. 文物承载着历史的记忆。如图所示河北博物院收藏文物中由金属材料制成的是
A. 中山王铁足铜鼎B. 民国三足玉熏炉
 C. 五代彩绘石质浮雕D. 元青花云龙纹瓷食盒
C. 五代彩绘石质浮雕D. 元青花云龙纹瓷食盒
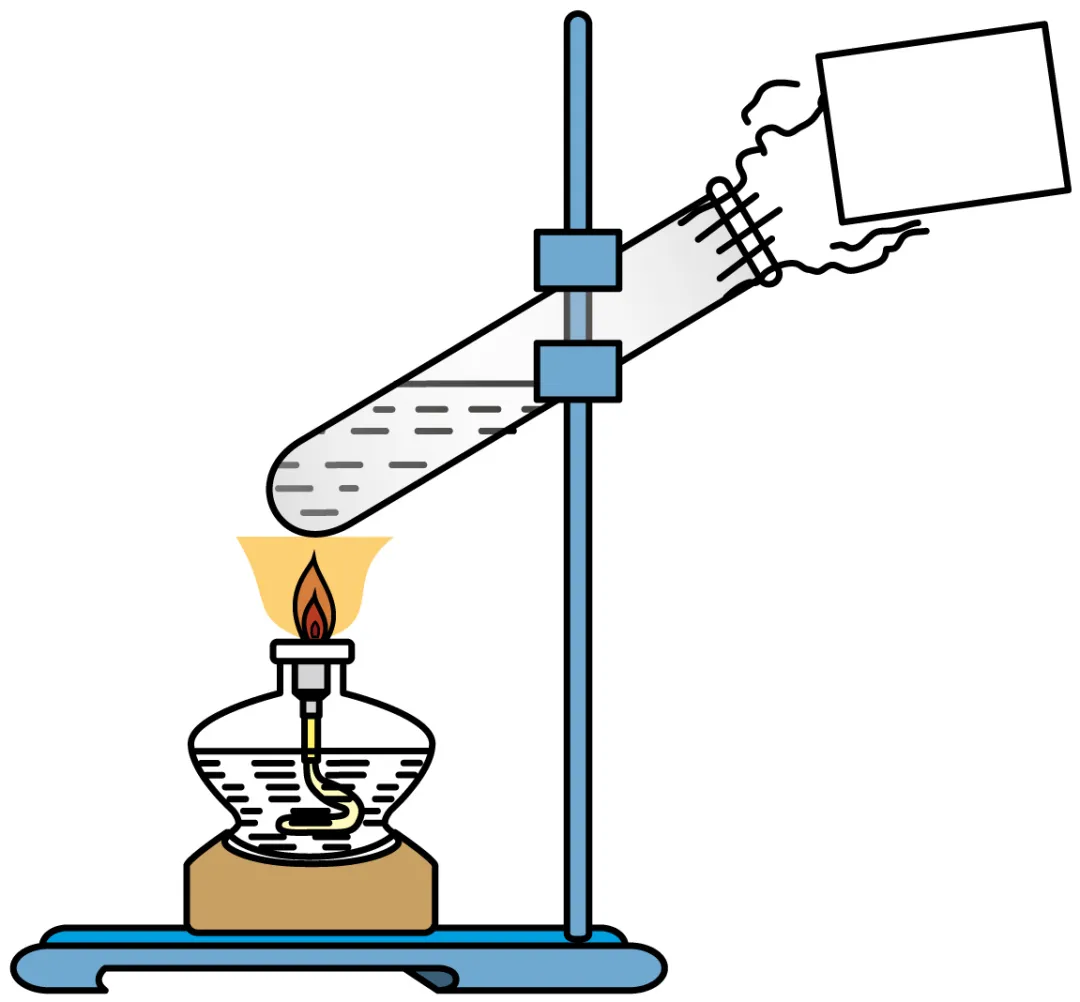
2. 如图所示为“水的沸腾”实验,其中没有用到的仪器是
A. 酒精灯B. 烧杯C. 铁架台D. 试管
3. 下列劳动实践的化学解释错误的是
A. 湿衣服夏天晾晒比冬天干 快——温度越高,分子运动越快
快——温度越高,分子运动越快
B. 铁锅洗净后擦干保存——铁在潮湿的空气中易生锈
C. 炒菜时用加碘食盐调味——适量补碘元素能预防贫血
D. 干冰用于易变质食物的短期保鲜——干冰升华吸热
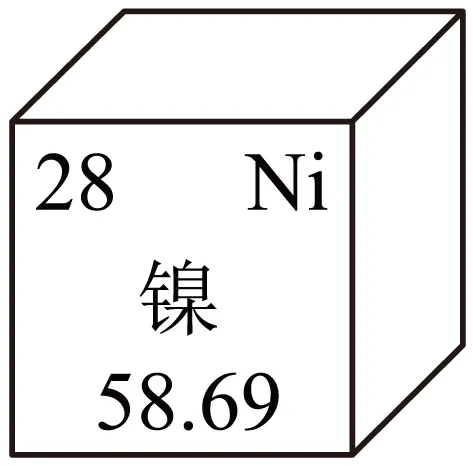 我国科研团队创新性地实现了“纳米负能界面强化镍基合金”的制备,使材料强度逼近理论极限,如图所示为元素周期表中镍元素的信息。下列说法正确的是
我国科研团队创新性地实现了“纳米负能界面强化镍基合金”的制备,使材料强度逼近理论极限,如图所示为元素周期表中镍元素的信息。下列说法正确的是
A. 镍属于非金属元素B. 镍合金的硬度比镍低
C. 镍原子的质量为58.69gD. 镍原子的质子数为28
5. 下列有关资源的说法错误是
A. 回收利用废旧金属既能节约金属资源,又能节约能源
B. 空气中的稀有气体化学性质不活泼,用途不大
C. 水能参与很多化学反应,本身就是一种化学资源
D. 综合利用煤、石油等化石燃料可以得到塑料、合成纤维等合成材料
6. 产自河北灵寿的太行龙井茶是河北省农科院“南茶北移”的科研成果。龙井茶中含有的儿茶素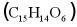 具有增强免疫力和预防心脑血管疾病等功效。下列关于儿茶素的说法中错误的是
具有增强免疫力和预防心脑血管疾病等功效。下列关于儿茶素的说法中错误的是
A. 龙井茶不能替代治疗心脑血管疾病的药物
B. 儿茶素由三种元素组成
C. 儿茶素中氢元素和氧元素的质量比为7:48
D. 儿茶素分子由15个碳原子、14个氢原子和3个氧分子构成
7. 分类是化学中常用的思维方法。下列物质的分类中正确的是
A. 纯净物:小苏打 、生石灰 、酒精B. 氧化物:氧气 、氧化汞、水
C. 单质:水银、氢气 、 生铁D. 可回收物:旧书、塑料瓶、果皮
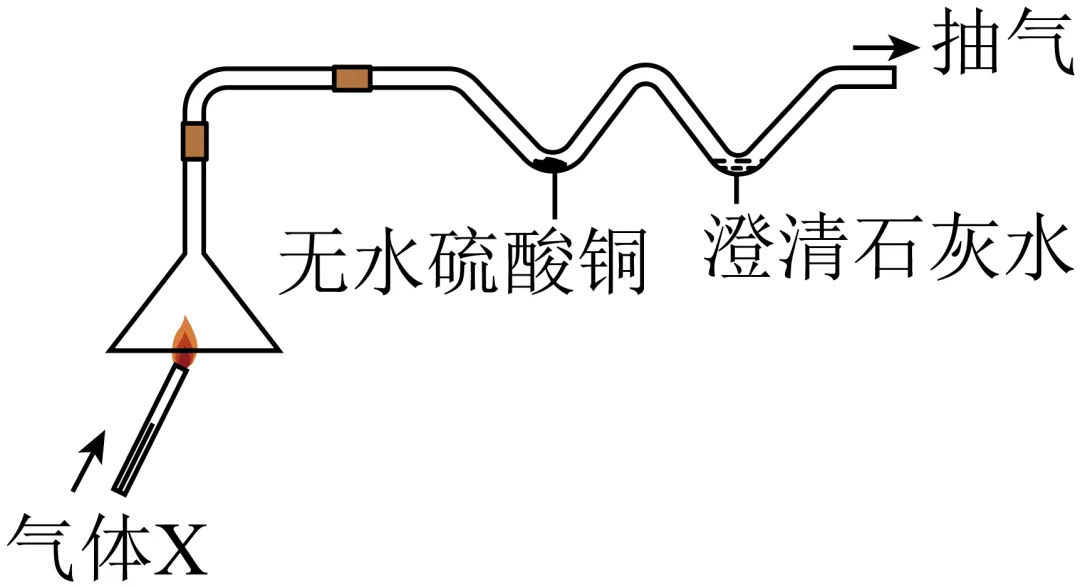 气体X可能是氢气、甲烷中的一种或两种,用如图所示装置验证其物质组成(无水硫酸铜为白色粉末,遇水变蓝)。下列分析错误的是
气体X可能是氢气、甲烷中的一种或两种,用如图所示装置验证其物质组成(无水硫酸铜为白色粉末,遇水变蓝)。下列分析错误的是
A 若仅观察到无水硫酸铜变蓝,则火焰呈淡蓝色
若仅观察到无水硫酸铜变蓝,则火焰呈淡蓝色
B. 若澄清石灰水变浑浊,则无水硫酸铜一定变蓝
C. 若无水硫酸铜变蓝,则气体X中一定含有氢气
D. 该实验利用气体X燃烧的产物推断物质的元素
9. 下列实验方案能达到实验目的的是
选项 | 实验目的 | 实验方案 |
A | 除去氧气中的水蒸气 | 将混合气体通过足量的稀硫酸 |
B | 区分棉纤维和羊毛纤维 | 分别点燃,观察燃烧时的现象和产物的状态 |
C | 分离氧化钙和碳酸钙 | 加水溶解,过滤、洗涤、干燥 |
D | 除去稀盐酸中少量的硫酸 | 加入过量的 BaCl2溶液,过滤 |
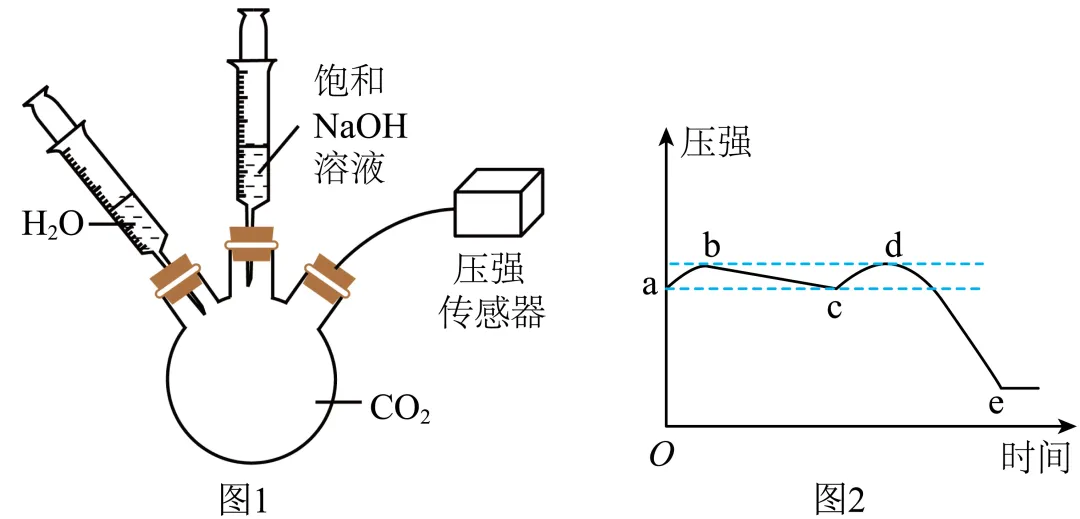 利用如图1所示实验证明氢氧化钠溶液和二氧化碳能发生化学反应。实验步骤:将注射器中的V mL水注入三颈烧瓶,一段时间后,将V mL饱和NaOH溶液注入三颈烧瓶。烧瓶中压强随时间变化如图2所示。下列说法错误的是
利用如图1所示实验证明氢氧化钠溶液和二氧化碳能发生化学反应。实验步骤:将注射器中的V mL水注入三颈烧瓶,一段时间后,将V mL饱和NaOH溶液注入三颈烧瓶。烧瓶中压强随时间变化如图2所示。下列说法错误的是
A. ab段压强增大是因为加入的水将瓶内气体压缩
B. bc段压强减小是因为CO₂溶于水且与水发生化学反应
C. de段溶液的质量减小
D. 对比曲线中 bc段和 de段,可以说明二氧化碳和氢氧化钠反应
二、非选择题(本大题共 8 小题,共 40 分)
11. 《天工开物》系统地总结了中国古代农业和手工业生产方面的重要成就,体现了古代劳动人民的智慧。
(1)有关煤的描述为“取煤烧之,火力甚烈。”煤属于___________(填“可再生”或“不可再生”)能源。可通过___________的方法使煤充分燃烧以增大火力。
(2)有关制取蔗糖的记载为“轧蔗取浆,煎汁成糖”。古人将甘蔗压榨取汁,过滤后加热浓缩,冷却后得到蔗糖晶体。从甘蔗中提取蔗糖的过程主要发生___________(填“物理”或“化学”)变化。“煎汁成糖”与实验室中___________操作的原理相同。
12. 中国空间站再生式环控生保系统已实现水氧闭环再生,高效水循环与二氧化碳还原技术为航天员长期在轨驻留提供稳定氧气与饮用水保障。
(1)空间站的水循环系统,将航天员的生活废水、冷凝水等进行处理,最终转化为纯净水。活性炭因具有___________性,用于航天水循环系统的预处理阶段以除去水中色素和异味。电解水可重新生成氧气供航天员呼吸使用。电解水的化学方程式为___________。
(2)空间站中,航天员呼出的二氧化碳与电解水产生的氢气在催化剂作用下转化为水,实现水资源再生。该反应的化学方程式为:CO2+4H2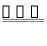 2H2O+X,X的化学式为___________。
2H2O+X,X的化学式为___________。
(3)空间站的水循环系统体现了航天领域对资源的循环利用。请结合生活实际,写出一条日常生活中节水或水资源循环利用的措施___________。
13. 口服补液盐散是治疗腹泻脱水的常用固体药剂,图1为某口服补液盐散的使用说明,图2所示为该口服补液盐散成分中氯化钠和氯化钾的溶解度曲线
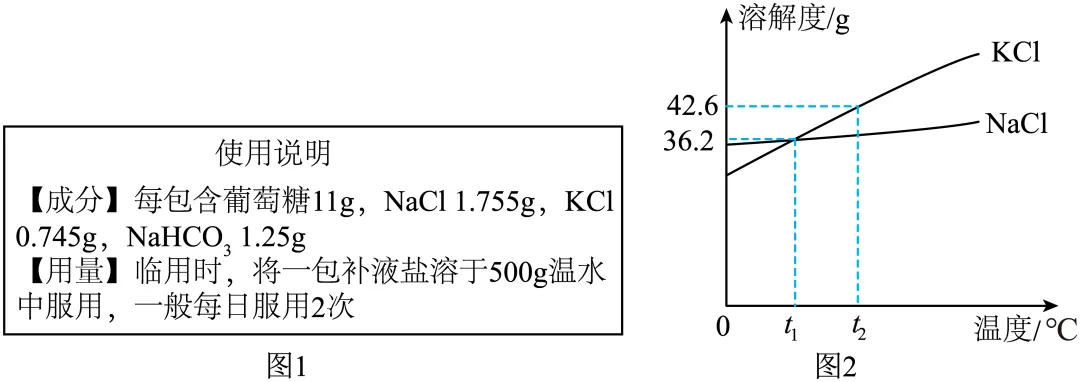
(1)口服补液盐散中,能为人体提供能量的物质是___________。
(2)___________℃时,氯化钾和氯化钠的溶解度相同。
(3)t2℃时,等质量的氯化钠和氯化钾配成该温度下的饱和溶液,需要水量更多的是___________。
(4)t2℃时,将一包补液盐散加入50g水中充分溶解,此时形成的氯化钾溶液是___________(填“饱和”或“不饱和”)溶液。
(5)一包补液盐散因密封不严受潮,吸收少量水分后结块。若仍按说明书加入500g温水冲服,充分溶解后,溶液中碳酸氢钠的溶质质量分数与未受潮药剂相比,会___________(填“变大”“变小”或“不变”)。
14. 甲醇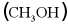 作为燃料应用于汽车领域,有助于推动能源结构优化。可利用工业尾气中
作为燃料应用于汽车领域,有助于推动能源结构优化。可利用工业尾气中 二氧化碳及焦炉气中的氢气合成甲醇和水,该化学反应的微观示意图如图所示。
二氧化碳及焦炉气中的氢气合成甲醇和水,该化学反应的微观示意图如图所示。
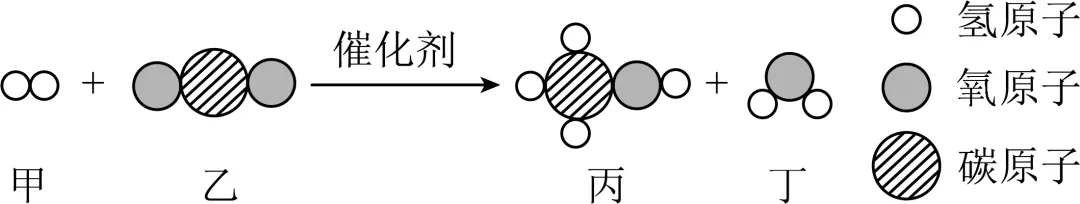
 请回答下列问题:
请回答下列问题:
(1)该反应过程中,没有发生变化的微观粒子是_____(填“分子”或“原子”)。
(2)该反应的化学方程式为___________。
(3)该反应能够缓解的环境问题是___________。
(4)甲醇燃烧时,化学能转化为___________能。
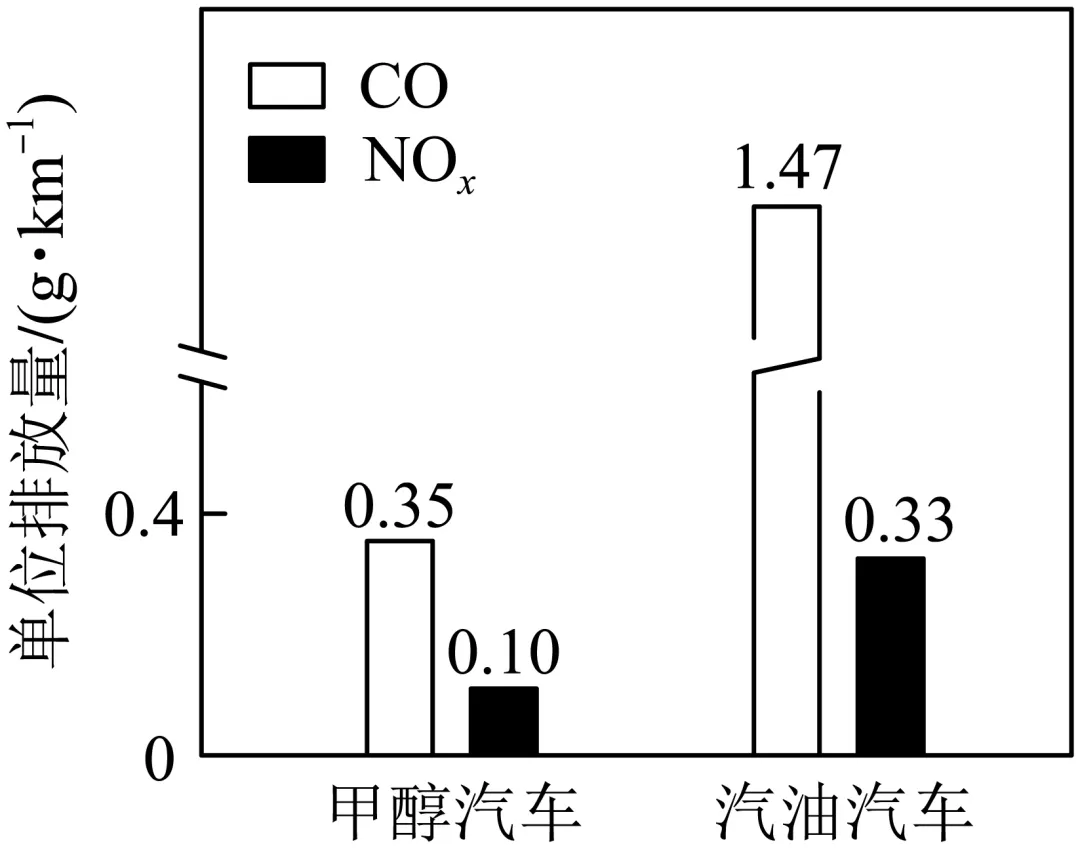
(5)如图所示为甲醇、汽油汽车的单位排放量。CO单位排放量较高的是___________汽车。
15. 波尔多液是农业上常用的杀菌剂,新配制的波尔多液呈微碱性,当其pH控制在7.5~9.0时,既能保证核心杀菌成分的稳定性,又能减少对作物的药害风险。小组同学设计了以废弃铜料(只含有铜和一定量的铁)和石灰乳为原料制备波尔多液的实验方案,如图所示。
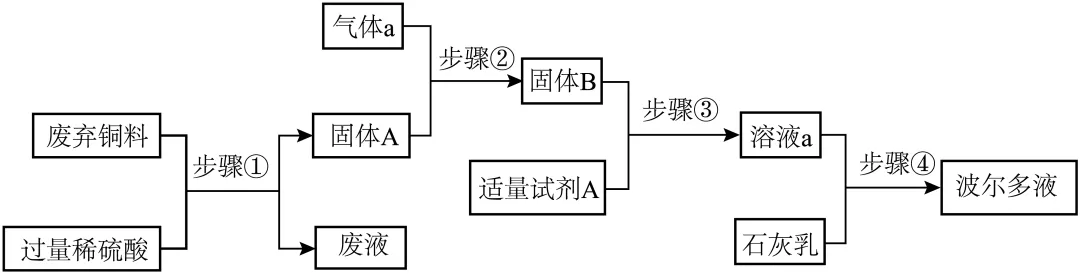
请回答下列问题:
(1)步骤①中过滤时,用到的玻璃仪器有玻璃棒、烧杯和___________。所得废液中的溶质为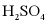 和___________(写化学式)。
和___________(写化学式)。
(2)步骤②中发生反应的化学方程式为___________。
(3)能说明步骤③中试剂A适量的实验现象为___________。
(4)步骤④中配制波尔多液时石灰乳不能过量,原因为___________。
16. 根据图1、2所示实验回答下列问题:
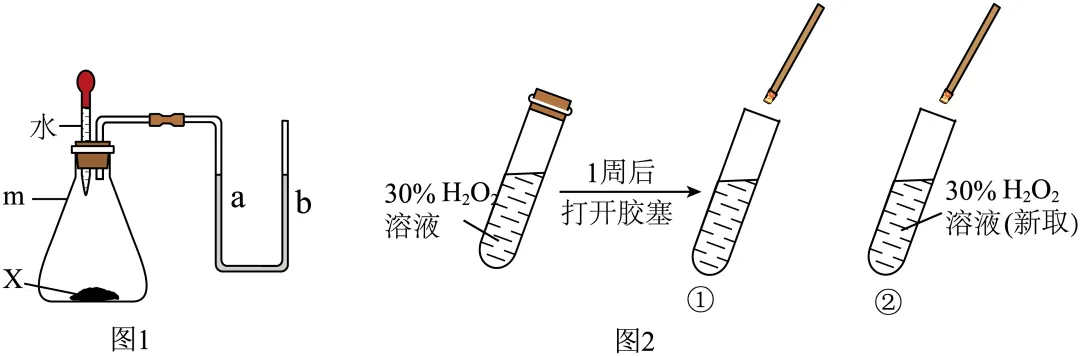
(1)图1为验证物质溶解时吸放热现象的实验。仪器m的名称为___________。U形管内 a、b液面相平,挤压胶头滴管,将水挤压进入m内,一段时间后观察到a侧液面低于b侧液面。X可能为___________。
(2)图2为探究过氧化氢分解的实验。向①、②试管中伸入带火星的木条,只有①中带火星的木条复燃,这是因为___________。要使②中带火星的木条伸入后立即复燃,可采取的措施是___________。该实验说明氧气具有的性质为___________。
 苹果是我国重要的经济作物之一,苹果树最适宜生长在pH为6.0~7.5的土壤中,土壤的酸碱性会对苹果品质产生重要影响。兴趣小组围绕果园土壤的酸碱度进行了系列探究活动。
苹果是我国重要的经济作物之一,苹果树最适宜生长在pH为6.0~7.5的土壤中,土壤的酸碱性会对苹果品质产生重要影响。兴趣小组围绕果园土壤的酸碱度进行了系列探究活动。
活动一:测定土壤的酸碱度
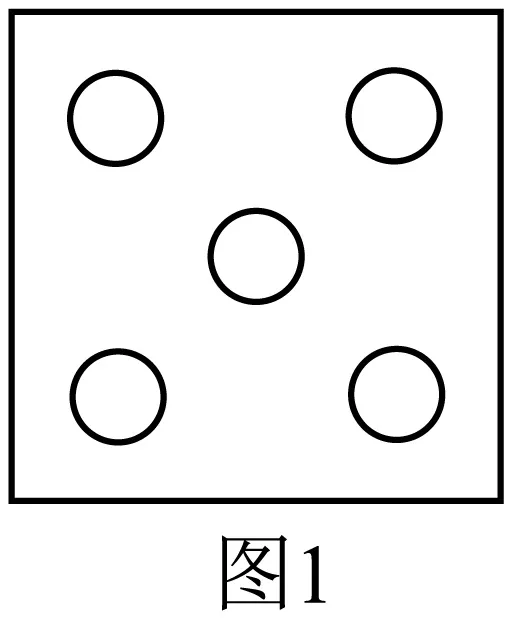
科学取样。在果园里按照图1所示的位置进行取样。
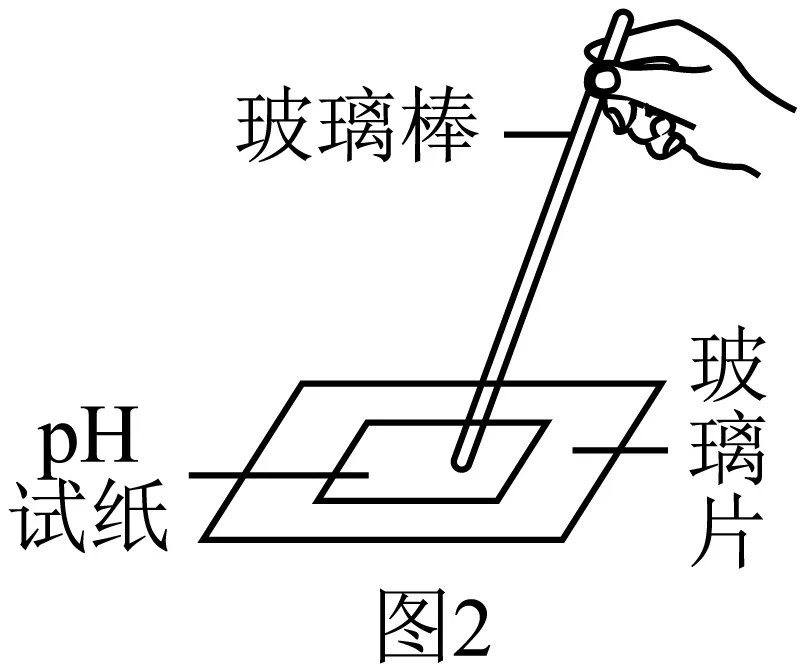 测定土壤酸碱度。将果园土壤样品与蒸馏水按照一定比例混合,充分振荡,静置,得土壤浸出液。用___________(填“用水润湿”或“干燥”)的pH试纸测定浸出液的酸碱度(图2),测得pH>7,该地土壤呈碱性。用pH计进一步测量,测得该土壤浸出液的pH为8.6。
测定土壤酸碱度。将果园土壤样品与蒸馏水按照一定比例混合,充分振荡,静置,得土壤浸出液。用___________(填“用水润湿”或“干燥”)的pH试纸测定浸出液的酸碱度(图2),测得pH>7,该地土壤呈碱性。用pH计进一步测量,测得该土壤浸出液的pH为8.6。
活动二:探究土壤呈碱性的原因
(2)调查发现,当地农民曾将草木灰(主要成分为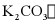 水溶液呈碱性)和
水溶液呈碱性)和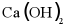 使用在果园中。
使用在果园中。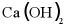 的俗称为___________。
的俗称为___________。
【提出问题】导致土壤呈碱性 物质是什么?
物质是什么?
【做出猜想】K2CO3、 Ca(OH)2或KOH中的一种或两种。
【进行实验】
实验步骤 | 实验现象 |
步骤1:将土壤浸出液加热浓缩,向其中加入过量的稀盐酸 | 有气泡产生 |
步骤 2:另取少量土壤浸出液的浓缩液,向其中加入过量氯化钙溶液(呈中性) | 有白色沉淀生成 |
步骤3:向步骤2的上层清液中滴加酚酞溶液 | 溶液变红色 |
 交流讨论】(3)步骤1中,产生气泡的化学方程式为___________。
交流讨论】(3)步骤1中,产生气泡的化学方程式为___________。
(4)步骤3中,溶液变红色是因为上层清液中含有的微观粒子是___________(用符号表示)。
【得出结论】(5)导致该土壤呈碱性的物质是___________。
活动三:确定改良土壤碱性的方法
【查阅资料】硫酸亚铁、硫酸铵和磷酸二氢钾都是土壤pH调节剂,改良1m3碱性土壤的施用数据如下表所示。
土壤pH调节剂 | 用量(kg) | 总价(元) | 施用60天后最大pH降低幅度 |
硫酸亚铁 | 4 | 6.4 | 2.28 |
硫酸铵 | 5 | 7.5 | 1.8 |
磷酸二氢钾 | 6 | 58.8 | 0.69 |
【分析讨论】
(6)欲使该果园土壤的pH从8.6调至 6.0~7.5,最适宜的土壤调节剂是___________。
【拓展延伸】(7)硫酸铵和磷酸二氢钾是常见的化肥,其中___________属于复合肥。
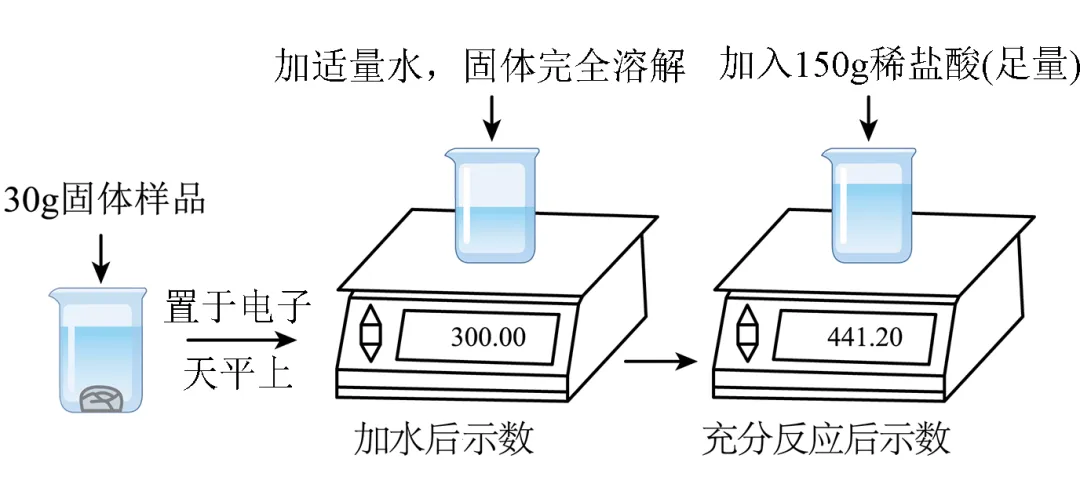
18. 某网红瓜果清洗剂“苏打盐”的组成成分为 NaHCO3和NaCl。为测定该“苏打盐”样品中 NaHCO3的含量,小组同学进行了如图所示实验:
请回答:
(1)产生CO2气体的质量为___________g。
(2)该“苏打盐”样品中NaHCO3的质量分数。(要求有必要的化学方程式和计算步骤)
答案1-5.ABCDB6-10.DACBC
11.(1)①. 不可再生②. 将煤粉碎(或鼓入足量空气)(2)①. 物理②. 蒸发结晶
12.(1)①. 吸附②. 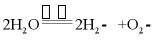 (2)CH4(3)用洗菜水浇花(合理即可)
(2)CH4(3)用洗菜水浇花(合理即可)
13.(1)葡萄糖(2)t1(3)氯化钠(4)不饱和(5)变小
14.(1)原子(2)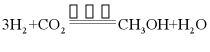 (3)温室效应(4)热##内(5)汽油
(3)温室效应(4)热##内(5)汽油
15.(1)①. 漏斗②. FeSO4(2)2Cu+O2 2CuO(3)固体恰好完全溶解
2CuO(3)固体恰好完全溶解
(4)石灰乳过量会使波尔多液pH过高,产生药害且降低杀菌效果
16.(1)①. 锥形瓶②. 氢氧化钠(合理即可)(2)①. 过氧化氢溶液常温下分解速度慢,②试管时间短,过氧化氢分解产生氧气很少②. 加入二氧化锰(合理即可)③. 支持燃烧
17.(1)干燥(2)熟石灰##消石灰
(3)K2CO3+2HCl=2KCl+H2O+CO2↑
(4)OH⁻(5)K2CO3、Ca(OH)2##K2CO3、KOH
(6)硫酸亚铁(7)磷酸二氢钾
18.(1)8.8(2)解:设样品中NaHCO3的质量为x,则
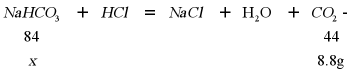
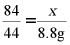
解得:x=16.8g
NaHCO3的质量分数为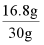 ×100%=56%
×100%=56%
答:样品中NaHCO3的质量分数为56%。